Tác dụng của thuốc giải lo âu trong việc điều trị các triệu chứng tâm thần kinh còn sót lại sau khi nhiễm COVID-19
Tác dụng của thuốc giải lo âu trong việc điều trị các triệu chứng tâm thần kinh còn sót lại sau khi nhiễm COVID-19
E.A. Alexandrova1, dalex1970@mail.ru, E.V. Parshina, I.V. Borodacheva1, A.G. Suslov2, K.M. Belyakov1, V.S. Yulin1, S.V. Fomin1
Bệnh viện đa khoa Khu vực Nizhny Novgorod mang tên N.A. Semashko; 603126, Nga, Nizhny Novgorod, đường Rodionova, nhà 1901
Bệnh viện đa khoa thành phố số 39; 603028, Nga, Nizhny Novgorod, đường cao tốc Moscow, 1442
Người dịch: PGS.TS.BS. Nguyễn Văn Tuấn – Bộ môn tâm thần, ĐH Y Hà Nội
TÓM TẮT
Giới thiệu. Ngoài các biểu hiện tiến triển cấp tính, nhiễm coronavirus còn kèm theo các triệu chứng kéo dài (suy nhược, biểu hiện triệu chứng tâm thần qua cơ thể, rối loạn giấc ngủ và nền tảng tâm lý cảm xúc), việc điều trị để điều chỉnh các biểu hiện này là đặc biệt cấp thiết.
Mục đích nghiên cứu. Nghiên cứu các khía cạnh về tâm lý, cơ thể và nhận thức của rối loạn lo âu sau khi nhiễm coronavirus, trong quá trình điều trị bằng tofisopam (Grandaxin®) liều 150 mg / ngày.
Tài liệu và phương pháp. Trong nghiên cứu có sự tham gia của các bệnh nhân đã trải qua đợt nhiễm coronavirus chủng mới, những người mà 4 tuần sau khi kết thúc điều trị có những dấu hiệu bất ổn cho phép đặt giả thiết về sự hiện diện của rối loạn lo âu. Thang điểm Hamilton được sử dụng để đánh giá mức độ lo âu. Bệnh nhân được thăm khám trước khi bắt đầu điều trị, sau 2 tuần, sau 4 tuần và sau 6 tuần áp dụng liệu pháp điều trị.
Kết quả. Trước khi bắt đầu điều trị, tất cả các bệnh nhân đều có tổng mức lo âu cao: điểm HAM-A trung bình là 31,72 ± 2,24 điểm. Khi kết thúc liệu trình điều trị bằng Grandaxin®, tất cả bệnh nhân đều giảm mức độ lo âu: điểm HAM-A trung bình là 12,68 ± 2,04 điểm (p<0,001). Khi kết thúc liệu trình, các bệnh nhân ghi nhận sự gia tăng khả năng hoạt động trí óc, cải thiện trí nhớ và chú ý, tức là giảm rõ rệt mức độ nghiêm trọng của rối loạn nhận thức liên quan đến lo âu, điểm trung bình theo thang điểm phụ “suy giảm nhận thức” giảm ba lần, từ 1,6 ± 0,12 còn 0,5 ± 0,09 (p<0,001).
Kết luận. Việc rối loạn nền tảng tâm lý – cảm xúc (thường xảy ra dưới dạng gia tăng lo âu cá nhân), rối loạn giấc ngủ, rối loạn hệ thần kinh thực vật, hội chứng suy nhược ảnh hưởng đáng kể đến chất lượng cuộc sống của những bệnh nhân sau mỗi đợt nhiễm coronavirus. Cần có một phương pháp tiếp cận tổng hợp trong chẩn đoán lâm sàng về hậu quả lâu dài của mỗi đợt nhiễm coronavirus chủng mới và việc điều chỉnh các hậu quả này sau đó bằng liệu pháp điều trị bằng thuốc.
Từ khóa: suy nhược, lo âu, rối loạn hệ thần kinh thực vật, rối loạn giấc ngủ, COVID-19, tofisopam.
Trích dẫn: Alexandrova E.A., Parshina E.V., Borodacheva I.V., Suslov A.G., Belyakov K.M., Yulin V.S., Fomin S.V. Tác dụng của thuốc giải lo âu trong việc điều trị các triệu chứng tâm thần kinh còn sót lại sau khi nhiễm COVID-19. Medical Council. 2021;(12):50–60. (In Russ.). https://doi.org/10.21518/2079-701X-2021-12-50-60.
Xung đột lợi ích: Các tác giả tuyên bố không có xung đột lợi ích.
GIỚI THIỆU
Vào cuối năm 2019, một đợt bùng phát dịch bệnh do coronavirus chủng mới gây ra đã xảy ra ở Cộng hòa Nhân dân Trung Hoa (CHND Trung Hoa) với tâm dịch tại Vũ Hán. Vào ngày 11 tháng 2 năm 2020, Tổ chức Y tế Thế giới (WHO) đã ấn định tên chính thức của bệnh nhiễm trùng do coronavirus chủng mới gây ra là COVID-19 (“Bệnh do Coronavirus 2019”).
Tính cấp thiết của việc nghiên cứu các hậu quả về mặt tâm thần kinh trong nhiễm trùng do coronavirus chủng mới là do sự ảnh hưởng đáng kể của bệnh tới chất lượng cuộc sống của bệnh nhân. Ngoài ra, hiện tại, cần nghiên cứu thêm về ý nghĩa lâm sàng các hậu quả lâu dài của bệnh nhiễm trùng do coronavirus chủng mới, cũng như các nguyên tắc điều chỉnh thuốc điều trị.
Đại dịch SARS-CoV-2 (COVID-19) đã gây ra tỷ lệ mắc và tử vong chưa từng có trên toàn thế giới. Sau thời kỳ cao điểm của đại dịch, các dịch vụ y tế tập trung vào việc lên kế hoạch cho các chương trình phục hồi chức năng cho các bệnh nhân. Theo các tác giả từ nhiều nước khác nhau, thuật ngữ “hậu COVID cấp tính” đặc trưng bởi các triệu chứng dai dẳng 3 tuần sau khi nhiễm COVID-19, còn “COVID mãn tính” – đặc trưng bởi các triệu chứng kéo dài hơn 12 tuần. [1, 2].
Trong 1 nghiên cứu các bệnh nhân người Ý, 2 tháng sau khi điều trị nội trú khỏi Covid, 53% bệnh nhân nhận thấy mệt mỏi, 43% số bệnh nhân khó thở và 22% vẫn còn đau ngực. Trong một số nghiên cứu khác có báo cáo rằng tình trạng mệt mỏi dai dẳng sau 4-8 tuần hiện diện ở hơn 2/3 số người bị nhiễm coronavirus, sau đó là là đến triệu chứng khó thở và các triệu chứng của rối loạn PTSD [3].
Theo bảng phân loại bệnh quốc tế, bản sửa đổi thứ 10 (ICD-10), các tiêu chí chẩn đoán rối loạn lo âu lan tỏa (F41.1) là các biểu hiện về cơ thể (hệ thần kinh tự trị), thể hiện qua một loạt các rối loạn quan trọng sống còn đối với bệnh nhân: tim mạch, hô hấp, thần kinh, tiêu hóa, sinh dục, điều nhiệt, vận động [4].
Như đã biết, rối loạn chức năng của một số hệ thống não bộ đóng vai trò quan trọng trong cơ chế bệnh sinh của các rối loạn tâm thần: hệ thống limbic, cấu tạo lưới của thân não, quá mẫn cảm của các cấu trúc trung tâm đối với hoạt động hệ thần kinh tự trị.
Nhiễm COVID-19 ảnh hưởng đến hệ thống thần kinh tự trị, vừa là yếu tố trực tiếp làm hỏng cấu trúc của hệ thống thần kinh tự trị, vừa kích hoạt cơ chế nhận cảm căng thẳng bất thường và gây rối loạn căng thẳng sau chấn thương [5]. Được biết, “cơn bão cytokine” trong COVID-19 có liên quan đến việc kích hoạt hệ thần kinh giao cảm, trong số các cơ chế khác, thúc đẩy việc giải phóng các cytokine gây viêm. Đồng thời, việc kích thích dây thần kinh phế vị (phó giao cảm) dẫn đến phản ứng chống viêm (giảm mức yếu tố hoại tử khối u TNF-a), điều này cho thấy cần chú ý tới các mục tiêu điều trị khi có rối loạn chức năng của hệ thần kinh tự trị [6, 7].
Rối loạn chức năng dinh dưỡng của tế bào não liên quan đến COVID-19, có thể do chính virus gây ra. Các hội chứng thần kinh qua trung gian miễn dịch đã được mô tả [8].
Người ta cũng biết rằng các rối loạn thần kinh thực vật như hạ huyết áp thế đứng và chứng tim đập nhanh tư thế có liên quan đến tự kháng thể [9].
Vì vậy, các thụ thể a/β -adrenergic và thụ thể muscarinic có thể được kích thích bởi các tự kháng thể cụ thể [10]. Do đó, cơ chế tự miễn dịch đối dẫn đến các rối loạn hoạt động thần kinh có thể đóng vai trò quan trọng [3].
Một số cách thức xâm nhập của coronavirus vào các trung khu của hệ thần kinh thực vật được thảo luận: sự chuyển đổi từ vùng hầu đến các tế bào khứu giác và sâu hơn vào thân não, tiếp đó là tới các cấu tạo khác của hệ thần kinh trung ương thông qua sự di chuyển qua synap. Ngoài ra qua đường máu, với các cơ chế khi có cả tổn thương hàng rào máu não. Có một cơ chế nữa cho thấy sự xâm nhập của vi rút qua dây thần kinh phế vị [11].
Ngay cả sau khi đã qua giai đoạn cấp tính của nhiễm coronavirus, bệnh nhân có nhiều triệu chứng kéo dài. Hầu hết bệnh nhân (lên đến 53,1%) cảm thấy mệt mỏi về tinh thần và thể chất [12-16] và các rối loạn khác như liên quan đến thiếu chú ý và giảm kiểm soát nhận thức [17, 18].
GABA (axit γ-aminobutyric) là chất dẫn truyền thần kinh ức chế chính trong hệ thần kinh của con người và đóng vai trò quan trọng trong hầu hết các tế bào thần kinh mã hóa và xử lý thông tin trong não. SICI (ức chế vỏ não ngắn hạn) và LICI (ức chế vỏ não dài hạn) bị suy giảm ở các bệnh nhân sa sút trí tuệ trán – thái dương, biểu hiện bằng rối loạn chức năng điều hành [15]. Các chức năng nhận thức khác nhau, chủ yếu là các chức năng điều hành, nhạy cảm với nồng độ GABA của não trong vỏ não trước trán [19, 20]. Sự gián đoạn hoạt động của hệ GABA trong con đường vỏ não có thể là nền tảng của các rối loạn đối với tất cả bệnh nhân. Với kích thích từ xuyên sọ đã chứng minh rằng sự giảm hoạt động hệ GABA ở vùng M1 (vỏ não vận động chính) đối với những bệnh nhân đã khỏi COVID-19 có các biến chứng thần kinh đi kèm và có triệu chứng mệt mỏi lâu dài. Do đó, việc thiếu hụt sự hoạt động của hệ GABA ở bệnh nhân nhiễm coronavirus là thực tổn thực sự [21].
Sự giảm mức GABA trong não ở những bệnh nhân bị nhiễm coronavirus là do tác động của các cytokine (cytokine gây viêm từ ngoại vi vào hệ thần kinh trung ương hoặc sản xuất quá mức các cytokine do các microglia (là một loại tế bào thần kinh đệm được tìm thấy trong hệ thống thần kinh trung ương) hoạt hóa). Cơ chế có thể được trình bày như sau: sự xâm nhập của virus vào hệ thần kinh trung ương dẫn đến giải phóng các cytokine tiền viêm (TNF-a, IL-6, IL-1B), nitric oxide, prostaglandin E2 và các gốc tự do. Những chất này làm trầm trọng thêm quá trình apoptosis (chết tế bào theo chương trình) và làm hoại tử tế bào thần kinh trong hệ thống thần kinh trung ương, đặc biệt là ở các cơ quan khác nhau của hồi hải mã (hippocampus), gây ảnh hưởng đáng kể trong quá trình phát sinh bệnh động kinh (do chúng làm tăng mức glutamate và giảm GABA trong vỏ não và hồi hải mã.)
IL-Iβ, được biểu hiện trong các tế bào thần kinh đệm hình sao (astrocytes) và microglia hoạt động, tạo ra nồng độ glutamate cao nhất trong các synap thần kinh, và sự gia tăng giải phóng glutamate từ tế bào thần kinh đệm hình sao hoặc giảm tái hấp thu glutamate có thể dẫn đến tăng tính dễ bị kích thích của tế bào não, và rồi sẽ dẫn đến cạn kiệt GABA.
TNF-a là một cytokine chống viêm khác được giải phóng từ các tế bào microglia và astrocytes đang hoạt động. TNF-a làm tăng giải phóng glutamate từ glia và điều chỉnh các thụ thể AMPA [22]. Các thụ thể AMPA hoạt động quá mức sẽ hấp thụ quá nhiều ion canxi và gây nhiễm độc tế bào thần kinh. Thông qua cơ chế nội bào, TNF-a không chỉ làm tăng số lượng thụ thể glutamate mà còn làm giảm số lượng thụ thể GABA, do đó làm tăng tính hưng phấn của tế bào thần kinh.
IL-6 là một cytokine tiền viêm khác thường được tìm thấy với một lượng nhỏ trong hệ thần kinh trung ương bình thường. Tuy nhiên, kích thích tế bào microglia and astrocytes có thể dẫn đến tăng sản xuất IL-6. Các cytokine khác như TNF-a, IL-Iβ, IFN-y và IL-17 làm tăng hiệu quả và tăng sản xuất IL-6. Các nghiên cứu đã chỉ ra rằng IL-6 làm giảm điện thế hóa dài hạn (Long-term potentiation: là một quá trình củng cố các hoạt động điện thế mới diễn ra tại synap) và giảm sinh các tế bào não tại hồi hải mã [23].
Một thử nghiệm đã chỉ ra rằng việc sử dụng GABA có thể ngăn ngừa các hậu quả nghiêm trọng của nhiễm coronavirus [24].
Cơ sở lý luận để nghiên cứu ảnh hưởng của tofisopam (Grandaxin®) trên các khía cạnh khác nhau của rối loạn lo âu sau khi nhiễm coronavirus là do benzodiazepine, đặc biệt là lorazepam, được sử dụng thậm chí để làm giảm các biểu hiện mê sảng ở bệnh nhân nhiễm coronavirus trong giai đoạn cấp tính, và nó đã được đưa vào các hướng dẫn lâm sàng. Người ta đã chứng minh rằng đối với những bệnh nhân bị COVID-19 và bị kích động nặng, việc sử dụng lorazepam kết hợp với thuốc chống loạn thần có thể tăng cường tác dụng an thần và giảm nguy cơ xuất hiện các triệu chứng ngoại tháp [25].
Thuốc benzodiazepine (phenazepam, alprazolam, lorazepam, v.v.) được sử dụng rộng rãi như một liệu pháp giải lo âu. Điều này là do khả năng giải lo âu của benzodiazepine để tăng cường hoạt động của GABA do điều biến allosteric của phức hợp GABA-ionophore. Thuốc benzodiazepine có nhiều tác dụng, bao gồm giải lo âu, an dịu, chống co giật, giãn cơ và giảm đau nhẹ [26, 27].
Đồng thời, thuốc an thần benzodiazepine còn có các tác dụng phụ như an dịu quá mức, suy giảm khả năng phối hợp, giảm chú ý, yếu cơ, giảm hoạt động, suy giảm chức năng nhận thức (CF), gây nghiện và hội chứng cai nghiện khi sử dụng kéo dài … Một nhiệm vụ cấp bách là tìm kiếm các loại thuốc không khác biệt về hiệu quả như benzodiazepine, nhưng đồng thời lại không có nhược điểm như benzodiazepine [27].
GRANDAXIN® (TOFISOPAM): CƠ CHẾ TÁC ĐỘNG VÀ PHẠM VI ỨNG DỤNG
Grandaxin® (tofisopam) do công ty Egis sản xuất đã được sử dụng rộng rãi trên toàn thế giới trong hơn 20 năm và nổi tiếng ở Nga.
Đặc điểm chính của nhóm thuốc Grandaxin® (tofisopam) là vị trí phân bố của nhóm nitơ. Nếu trong các thuốc benzodiazepine truyền thống, nhóm nitơ ở vị trí 1-4, thì trong Grandaxin và các thuốc tương tự, nó nằm ở vị trí 2-3, và do đó chúng thường được gọi là 2-3-benzodiazepine.
Do tính đặc hiệu của cấu trúc và về tính chất, thuốc có sự khác biệt đáng kể so với các benzodiazepine “cổ điển”. Tác dụng trên hệ thần kinh thực vật và giải lo âu của nó, không kèm theo gây an dịu và giãn cơ, đã làm cho nó có thể được ứng dụng rộng rãi trong các biểu hiện lâm sàng rõ rệt của lo âu trong phạm vi các bệnh tâm thần.
Chỉ định sử dụng Grandaxin® (tofisopam) là: điều trị các rối loạn tâm thần, các vấn đề tâm lý, kèm theo căng thẳng cảm xúc, lo âu, rối loạn hệ thần kinh tự chủ, thờ ơ, mệt mỏi và tâm trạng chán nản; hội chứng cai rượu.
Grandaxin® (tofisopam) ngày nay được đưa vào một số tiêu chuẩn chăm sóc sức khỏe ban đầu và chăm sóc đặc biệt, ví dụ, trong trường hợp các triệu chứng cai nghiện, tình trạng mất trí nhớ và nhiễm độc cấp tính do sử dụng các chất kích thần [28].
Việc sử dụng thang điểm và bảng câu hỏi có thể giúp xác định các rối loạn lo âu ngay cả ở những bệnh nhân không có phàn nàn riêng về bất ổn tâm lý. Trong chẩn đoán rối loạn lo âu, thang điểm Hamilton đã tự chứng minh rằng nó có thể phát hiện không chỉ các rối loạn cảm xúc mà còn cả các rối loạn tâm thần [29].
Mục tiêu của nghiên cứu: nghiên cứu các khía cạnh tâm lý, cảm giác và nhận thức của rối loạn lo âu sau khi nhiễm coronavirus, trong quá trình điều trị bằng Grandaxin.
TÀI LIỆU VÀ PHƯƠNG PHÁP
Các nghiên cứu lâm sàng được thực hiện tại Cơ sở y tế thuộc ngân sách nhà nước tỉnh Nizhegorod “Bệnh viện đa khoa tỉnh Nizhegorod mang tên N.A. Semashko”. Nghiên cứu có sự tham gia của 30 bệnh nhân đã trải qua một đợt nhiễm coronavirus mới, 4 tuần sau khi kết thúc điều trị, họ có những dấu hiệu cho phép đặt giả thiết về việc ở những bệnh nhân này có sự hiện diện của rối loạn lo âu.
Công trình này bản chất là một nghiên cứu quan sát mở, có triển vọng. Thiết kế nghiên cứu đề xuất đưa vào nhóm nam và nữ từ 18 đến 62 tuổi có kèm theo chứng rối loạn lo âu (TR), với mức độ lo âu ít nhất là 17 điểm theo thang điểm Hamilton. Tất cả các bệnh nhân đã ký đồng ý tham gia nghiên cứu. Trong thời gian quan sát và trong 3 tháng. trước khi đưa vào nghiên cứu, bệnh nhân không được dùng thuốc tác động lên hệ thần kinh thực vật và hướng thần. Grandaxin được kê đơn với liều hàng ngày 150 mg, chia làm 2 lần, trong 6 tuần. Mức độ lo âu được đánh giá bằng thang Hamilton. Thang điểm lo âu Hamilton (Hamilton Anxiety Scale) là thang đánh giá lâm sàng được thiết kế để đo mức độ nghiêm trọng của chứng rối loạn lo âu của bệnh nhân, bao gồm 14 chỉ số, mỗi chỉ số được xác định bởi một số triệu chứng như: tâm trạng lo âu, căng thẳng, sợ hãi, mất ngủ, suy giảm trí tuệ, khi sắc trầm, các triệu chứng hệ thần kinh thực vật, các triệu chứng tim mạch, hô hấp, tiêu hóa, niệu sinh dục và rối loạn hành vi khi thăm khám.
Trong Thang điểm lo âu Hamilton, mỗi chỉ số được đánh giá trên thang điểm 5, từ 0 điểm (không có) đến 4 điểm (nghiêm trọng). HAM-A được điền trong quá trình phỏng bệnh nhân, khi phỏng vấn cần thu thập tiền sử bệnh, đồng thời quan sát hành vi và các biểu hiện phi ngôn ngữ khác của các rối loạn tâm thần đang được nghiên cứu. Để có được tổng điểm phản ánh mức độ nghiêm trọng của chứng rối loạn lo âu, cộng tổng tất cả các điểm. Ngoài ra, đánh giá riêng 6 điểm đầu tiên của thang điểm, là biểu hiện lo âu về tinh thần, và 8 điểm còn lại là biểu hiện của lo âu về triệu chứng cơ thể. Sự biến động của từng chỉ số ở thang đo phụ trong quá trình điều trị được phân tích riêng.
Việc khám cho bệnh nhân được thực hiện trước khi bắt đầu điều trị, sau 2, 4 và 6 tuần thực hiện liệu pháp điều trị.
Xử lý dữ liệu thống kê được thực hiện bằng cách sử dụng gói phần mềm EXCEL và SPSS. Để mô tả dữ liệu thu được, sử dụng các tiêu chí thống kê mô tả: trung bình cộng, độ lệch tiêu chuẩn. Đánh giá sự khác biệt của các trị số trung bình đối với hai nhóm có sử dụng tiêu chí Wilcoxon. Sự khác biệt được coi là có ý nghĩa thống kê khi p <0,05.
KẾT QUẢ VÀ THẢO LUẬN
Đánh giá tác dụng của Grandaxin® đối với các biểu hiện lo âu về tâm lí và cơ thể trong quá trình phục hồi chức năng ở bệnh nhân sau khi nhiễm coronavirus chủng mới được thực hiện bằng cách sử dụng HAM-A. Trước khi bắt đầu điều trị bằng Grandaxin®, tất cả bệnh nhân đều có tổng mức lo âu cao: điểm HAM-A trung bình là 31,72 ± 3,2 điểm. Sau 2 tuần, mức độ lo âu giảm 18% là 25,88 ± 2,4. Sau 4 tuần tiếp theo, điểm trung bình HAM-A là 19,68 ± 2,7, thấp hơn 37% so với điểm ban đầu. Hết 6 tuần điều trị bằng Grandaxin®, tất cả bệnh nhân đều giảm mức độ lo âu: điểm HAM-A trung bình là 12,68 ± 2,04 điểm (p <0,001).
Hiệu quả tích cực rõ ràng của việc điều trị bằng Grandaxin® liên quan đến các biểu hiện lo âu về tâm lí theo mục 1-6 của HAM-A.
Trước khi bắt đầu điều trị, phát hiện việc gia tăng so với mức độ trước khi mắc bệnh, các biểu hiện lo âu và mất khả năng tập trung khi thực hiện các hoạt động hàng ngày và kỹ năng làm việc, tập trung quá mức vào việc xem tin tức liên quan đến lây nhiễm coronavirus chủng mới, mặt khác, hiểu rõ về mức độ lo âu gia tăng khi đối mặt với “tin xấu”. Đồng thời, người bệnh có biểu hiện lo âu quá mức khi bạn bè, người quen, họ hàng thông tin về bệnh. Bản thân người bệnh và thân nhân của họ nhận thấy rằng ngay cả khi người được hỏi đã bình phục, người bệnh vẫn làm phiền người thân bằng những cuộc gọi vô lý vào điện thoại di động để phàn nàn và kể về trải nghiệm của họ liên quan đến căn bệnh mà họ mắc phải, kể cả trong giờ làm việc, điều mà trước khi bị bệnh họ chưa bao giờ làm như thế, đưa ra nhiều phân tích vô căn cứ, ngoài các loại thuốc do bác sĩ kê đơn, họ cố gắng tự điều trị theo internet. Tất cả những điều này ảnh hưởng đáng kể đến chất lượng cuộc sống không chỉ của bệnh nhân mà còn của gia đình họ. Sự căng thẳng trong nội tâm được thể hiện qua việc mong đợi tin xấu, thậm chí đến mức phát hoảng nếu bệnh nhân không thể liên lạc kịp thời với người thân hoặc bạn bè mắc bệnh tương tự. Bệnh nhân hay cáu gắt, lo âu và hồi hộp khi giao tiếp với bác sĩ là những biểu hiện điển hình, bệnh nhân thường cố gắng buộc tội bác sĩ rằng họ “không hiểu những gì bệnh nhân phải trải qua”. Các nỗi sợ vừa có cơ sở – bị biến chứng sau một trận ốm, nỗi lo sợ cho cuộc sống của bạn bè, người thân và người quen, vừa không có cơ sở – “nghẹt thở trong giấc mơ và chết”, “tôi cảm thấy tim mình có thể đột ngột ngừng đập” với kết quả ECG và EchoS bình thường. Mặc dù nỗi sợ hãi có căn cứ hay không, trong mỗi trường hợp này, các rối loạn hành vi đã được ghi nhận, dẫn đến thực tế là ảnh hưởng tới trật tự cuộc sống thông thường và chất lượng cuộc sống của bệnh nhân. Đặc biệt, chính bệnh nhân đã gọi điện đến đường dây nóng coronavirus mà không có lý do, thông báo những tin nhắn quá xúc động của mình trên mạng xã hội và sau đó bày tỏ sự hối hận về sự thiếu kiểm soát của mình. Ngoài ra, bệnh nhân liên tục lau dọn căn hộ, bao gồm cả việc thường xuyên, lặp đi lặp lại một cách không cần thiết, sử dụng chất khử trùng, lau tay cầm và bề mặt làm việc, ngay cả khi không ai chạm vào những bề mặt này, điều mà bệnh nhân chưa làm trước đó.
Rối loạn trầm cảm được đặc trưng bởi tâm trạng chán nản, mất hứng thú, không quan tâm tới những sở thích trước đây, thức dậy sớm, trầm cảm, kết hợp với mong muốn nghiên cứu tin tức liên quan đến nhiễm coronavirus. Một biểu hiện điển hình của rối loạn trầm cảm là sự biến động hàng ngày của trạng thái trầm cảm vào các giờ buổi tối.
Đến cuối tuần thứ 6 áp dụng liệu pháp điều trị ở tất cả các bệnh nhân cho thấy biểu hiện bình thường hóa mức độ lo âu: điểm trung bình là 12,68±2,0 (p<0,001). Trong quá trình điều trị, đa số bệnh nhân giảm đáng kể lo âu, không còn lo âu về những “cảm giác tồi tệ”. Những thay đổi tích cực đáng kể đã được ghi nhận vào cuối tuần thứ 2 từ khi bắt đầu điều trị bằng Grandaxin® – chỉ số “tâm trạng lo âu” giảm xuống 1,88 ± 0,3 (p <0,001), và sau 4 tuần trị liệu là 1,2 ± 0,4 (p <0,001), thấp hơn 53% so với mức ban đầu. Đến cuối tuần thứ 6 “tâm trạng lo âu” đã giảm đáng kể – từ 2,6 ± 0,5 xuống 0,48 ± 0,09 điểm (p<0,001). Chỉ số “căng thẳng nội tại” giảm dần trong quá trình trị liệu, sau 2 tuần giảm xuống 2,04 ± 0,17 (p <0,001), sau 4 tuần giảm xuống 1,36 ± 0,16 (p <0,001). Và kết quả là vào cuối tuần điều trị thứ 6 bằng Grandaxin® giảm 3,5 lần – từ 2,6 ± 0,09 xuống 0,77 ± 0,08 điểm (p <0,001). Thực tế, nỗi sợ hãi không có động cơ đã biến mất, giảm từ 2,00 ± 0,12 đến 0,63 ± 0,09 điểm (p <0,001). Mức độ nghiêm trọng của chỉ số phụ “rối loạn trầm cảm” giảm 45% sau 4 tuần và đạt 1,32 ± 0,15 (p <0,001), còn vào cuối tuần thứ 6 từ khi bắt đầu điều trị, giảm từ 2,43 ± 0,09 xuống 0,9 ± 0,07 điểm (p <0,001).
Trước khi bắt đầu điều trị bằng Grandaxin®, phần lớn bệnh nhân, 19 trong số 30 (63%), bị rối loạn giấc ngủ rõ rệt, biểu hiện khó ngủ, rối loạn duy trì giấc ngủ, thường xuyên thức giấc, ngủ chập chờn và cảm giác ngủ không ngon. Đến cuối tuần điều trị thứ 2 bằng Grandaxin®, mức độ nghiêm trọng của chứng mất ngủ giảm ở một nửa số bệnh nhân, nhưng điều này liên quan đến những rối loạn giấc ngủ nghiêm trọng nhất. Với những người rối loạn giấc ngủ có mức độ nghiêm trọng, những biến đổi theo hướng tích cực ở nhóm bệnh nhân này không thể đạt được trong một liệu trình hai tuần. Đến cuối tuần thứ 4 sau khi bắt đầu điều trị, chỉ có 37% (11) bệnh nhân bị rối loạn giấc ngủ nhẹ, trong khi số còn lại bị rối loạn giấc ngủ trung bình. Các chỉ số của thang điểm mất ngủ có thay đổi rõ rệt với giá trị giảm lần lượt từ 2,76 ± 0,4 khi bắt đầu điều trị và còn 2,04 ± 0,2 (p <0,001) sau 2 tuần, 1,6 ± 0,5 (p <0,001) sau 4 tuần và đạt 0,92 ± 0,4 (p <0,001) khi kết thúc điều trị bằng Grandaxin®. Mức độ nghiêm trọng của chứng mất ngủ trong vòng 6 tuần điều trị giảm từ 2,76 ± 0,4 xuống 0,92 ± 0,4 điểm (p <0,001). Việc bình thường hóa thời gian và chất lượng giấc ngủ vào cuối tuần thứ 6 kể từ khi bắt đầu điều trị đã được ghi nhận bởi 10% bệnh nhân (3 người), 10% khác rối loạn giấc ngủ vẫn ở mức độ nghiêm trọng. Hầu hết các bệnh nhân không thể đạt được chất lượng giấc ngủ như trước khi bị nhiễm coronavirus, tuy nhiên, các bệnh nhân ngủ ngon hơn, rối loạn duy trì giấc ngủ biến mất và giấc ngủ buổi sáng được phục hồi, mặc dù vẫn khó đi vào giấc ngủ.
Rối loạn trầm cảm và rối loạn hoảng sợ là những rối loạn dai dẳng nhất trong các rối loạn tâm thần liên quan đến lo âu. Một liệu trình điều trị kéo dài hai tuần là không đủ, việc bình thường hóa các thông số này ở hầu hết bệnh nhân chỉ được ghi nhận vào cuối tuần thứ tư kể từ khi bắt đầu điều trị và chúng biến mất hoàn toàn trong vòng 5 tuần điều trị chỉ ở 27 % bệnh nhân (11 người). Đồng thời, cần lưu ý rằng mức độ phản ứng sợ hãi, ám ảnh ở những bệnh nhân còn lại không còn ảnh hưởng đến chất lượng cuộc sống và hành vi của bệnh nhân. Những nỗi sợ hãi này đã mang tính chất các sự việc trong cuộc sống, mặc dù vẫn biểu hiện bằng sự quan tâm đến cuộc sống và sức khỏe của những người thân, thể hiện bằng những lời kêu gọi tuân thủ các biện pháp phòng ngừa và tiêm chủng, liên quan đến chính bệnh nhân: các biện pháp phòng ngừa và tuân thủ các nguyên tắc sống lành mạnh. Cũng có thể nói về sự cải thiện tâm trạng, hết trầm cảm, khôi phục giấc ngủ buổi sáng, hết tâm trạng thất thường trong ngày.
Tác dụng của Grandaxin® cũng được thể hiện trong việc giảm mức độ nghiêm trọng của suy giảm nhận thức liên quan đến lo âu trên thang phụ “suy giảm nhận thức”. Trước khi bắt đầu điều trị, bệnh nhân chủ yếu phàn nàn về các rối loạn trong phạm vi công việc như: không có khả năng tập trung vào công việc, suy giảm khả năng duy trì sự chú ý chủ động, suy giảm khi chuyển đổi từ loại hoạt động này sang loại hoạt động khác, nhanh chóng mệt mỏi khi gắng sức trí tuệ. Suy giảm nhận thức biểu hiện rõ rệt trước khi bắt đầu điều trị chỉ ở 3 trong số 30 bệnh nhân (10%), nhưng đặc điểm của họ là dai dẳng nhất. Chỉ ở 7 bệnh nhân sau 2 tuần có sự gia tăng khả năng hoạt động trí óc, cải thiện các chức năng nhận thức: điểm trung bình của thang điểm “suy giảm nhận thức” giảm từ 1,6 ± 0,12 xuống 1,2 ± 0,11 (p> 0,05).
Sau 4 tuần. Sự cải thiện được ghi nhận ở 12 bệnh nhân, điểm trung bình giảm từ 1,6 ± 0,12 xuống 1,03 ± 0,09 (p> 0,05).
Sau khi kết thúc quá trình điều trị, bệnh nhân ghi nhận sự gia tăng khả năng hoạt động trí óc, cải thiện trí nhớ và sự chú ý, tức là giảm rõ rệt rối loạn nhận thức liên quan đến lo âu, điểm trung bình giảm 78% – từ 1,64 ± 0,12 xuống 0,36 ± 0, 09 (p <0,001).
Tác dụng tích cực của thuốc Grandaxin® cũng được nhận thấy đối với việc phục hồi các rối loạn dạng cơ thể (somatoform) liên quan đến rối loạn cảm xúc ở bệnh nhân suy nhược hậu covid.
Rối loạn triệu chứng cơ thể được biểu hiện bằng hội chứng đau, rối loạn trương lực cơ, biểu hiện xơ cơ, co giật cơ. Cần lưu ý rằng cơn đau có liên quan đến tình trạng tâm lí bất ổn và lo âu. Những biểu hiện này trước khi bắt đầu điều trị đã thể hiện rõ ở một nửa số bệnh nhân. 15 người còn lại có biểu hiện rối loạn về cơ bắp (đã nói ở trên) trung bình. Không ghi nhận trường hợp nào không có rối loạn cơ hoặc rối loạn mức độ nhẹ. Rối loạn cảm giác được biểu hiện bằng các chứng loạn cảm giác, chứng đau đầu, hội chứng chân không yên, dị cảm.
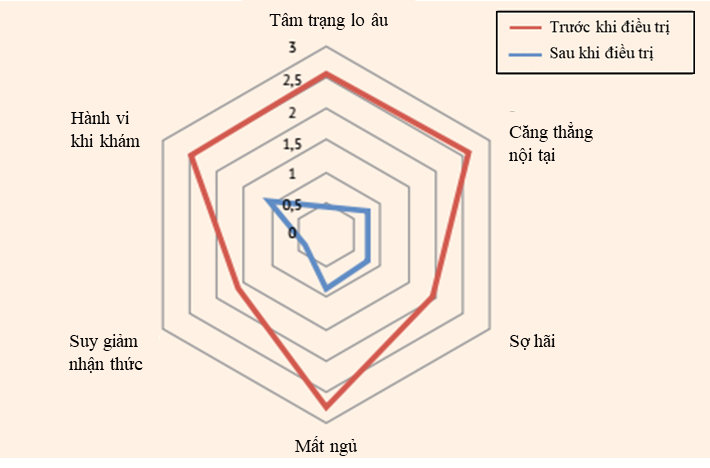
Đến cuối tuần thứ 2 mức độ nghiêm trọng của các rối loạn về cơ bắp giảm 30% từ 2,53 ± 0,09 xuống 1,77 ± 0,09, còn vào cuối tuần thứ 6 các triệu chứng giảm 2,5 lần: từ 2,53 ± 0,09 đến 1,13 ± 0,06 điểm (p<0,001). Không giống như rối loạn cơ, rối loạn nhận cảm (cảm giác) ít phản ứng hơn với sự điều trị. Vì vậy, mặc dù mức độ nghiêm trọng ban đầu thấp hơn, vào cuối tuần điều trị thứ 2, các biểu hiện chỉ giảm 17%: từ 2,23 ± 0,1 xuống 1,86 ± 0,1 điểm (p> 0,05), sau 4 tuần chỉ số này là 1,44 ± 0,15 (p <0,001), và vào cuối tuần thứ 6. cường độ các rối loạn giảm hơn 2 lần: từ 2,23 ± 0,09 xuống 0,97 ± 0,11 điểm (p <0,001). Tuy nhiên, khác với rối loạn về cơ bắp, rối loạn cảm giác chấm dứt hoàn toàn ở 6 bệnh nhân (20%) (Hình 1).
Thuốc bình thần, không giống như thuốc chống trầm cảm hoặc thuốc chống động kinh, không được coi là thuốc giảm đau cổ điển hoặc thuốc điều chỉnh rối loạn nhận cảm [30]. Tác dụng giảm đau của các benzodiazepin có tác động phụ thuộc vào liều lượng và không liên quan đến hệ thống opioid [31].
Tác dụng tăng cường của benzodiazepine khi sử dụng cùng với thuốc chống viêm không steroid (NSAID) đã được chứng minh [32]. Có bằng chứng cho thấy về hiệu quả cao hơn khi phối hợp sử dụng benzodiazepine với NSAIDS điều trị đau nửa đầu so với trị liệu chỉ dùng NSAID [33]. Vai trò của thụ thể benzodiazepine GABA của hệ thống nitroxydergic trong tác dụng giảm đau của benzodiazepine đã được thảo luận [34, 35].
Rối loạn chức năng thần kinh tự trị của hệ thống tim mạch trước khi bắt đầu điều trị với Grandaxin® được biểu hiện bằng nhịp tim nhanh, đánh trống ngực, cảm giác loạn nhịp của tim và huyết áp không ổn định. Sự biến đổi các chỉ số của “các triệu chứng tim mạch” ở thang điểm phụ không quá rõ ràng. Vì vậy, đến cuối tuần trị liệu thứ 2, chỉ số là 2,08 ± 0,6 (p> 0,05), và sau 4 tuần trị liệu, điểm số là 1,52 ± 0,7 (p> 0,05). Tuy nhiên, khi kết thúc điều trị, tần suất rối loạn tim mạch giảm 2 lần: từ 2,17 ± 0,11 xuống 1,06 ± 0,09 điểm (p<0,001). Ghi nhận giảm nhịp tim, giảm cảm giác khó chịu ở ngực, khó thở và “thiếu không khí”. Tuy nhiên, chỉ ở 3 bệnh nhân, các rối loạn tim mạch được chấm dứt hoàn toàn. Vào cuối quá trình điều trị với Grandaxin®, hầu hết bệnh nhân vẫn có xu hướng nhịp tim nhanh và huyết áp không ổn định, có giảm các triệu chứng tim chủ quan và giảm triệu chứng liên quan cảm xúc của họ.
Hình 1. Thay đổi các biểu hiện triệu chứng hệ thần kinh thực vật của lo âu trong quá trình điều trị bằng thuốc Grandaxin®
SARS-CoV-2 xảy ra như một bệnh lý huyết khối và mạch máu nhắm vào các tế bào nội mô khắp cơ thể, và đặc biệt rõ ràng ở những bệnh nhân mắc đồng thời các bệnh chuyển hóa tim mạch, đặc biệt là tăng huyết áp, có rối loạn chức năng nội mô đồng thời.
Rối loạn chức năng nội mô và các biến chứng về huyết khối được đặc trưng bởi sự ức chế tổng hợp nitric oxide nội mô (eNOS) khi kèm theo thiếu hụt nitric oxide đồng thời. Trong các mạch máu khỏe mạnh, nội mạc tiết ra một chất làm giãn mạch và chống huyết khối, oxit nitric. Ở các mạch máu bị tổn thương, quá trình này bị gián đoạn, góp phần làm tăng huyết áp và hình thành huyết khối. Quá trình phục hồi nitric oxide, không phụ thuộc vào eNOS, có thể chống lại viêm nội mạc và thúc đẩy giãn mạch phổi, chống huyết khối và tác dụng kháng virus trực tiếp.
Mặt khác, oxit nitric đã được báo cáo là gây trở ngại cho các tương tác giữa protein S của coronavirus và thụ thể vật chủ của nó, ACE-2.
S-nitrosyl hóa của protease cysteine của virus trung gian qua nitric oxide và protease serine của vật chủ, TMPRSS2, rất quan trọng đối với sự xâm nhập của virus vào tế bào, dường như nhạy cảm với nitric oxide [36].
Tiềm năng điều trị của oxit nitric được thảo luận trong một số nghiên cứu [37, 38, 39]. Tác dụng tốt có thể có của Grandaxin® có thể được liên kết với không chỉ tác dụng trên hệ thần kinh thực vật của nó liên quan đến sự cải thiện trong chuyển hóa GABA, mà còn có tác dụng tích cực trên hệ thống nitroxydergic. Đồng thời, cần lưu ý rằng các triệu chứng tim mạch được chúng tôi xem xét trong bối cảnh rối loạn lo âu hoàn toàn, trong khuôn khổ rối loạn chức năng tự trị, và tình trạng của hệ thống tim mạch sau khi nhiễm coronavirus cần được nghiên cứu thêm.
Các triệu chứng về hô hấp dưới dạng cảm giác không thể “hít thở sâu”, cảm giác thiếu không khí, sợ “ngạt thở”, đặc biệt là “khi ngủ”, những thay đổi về nhịp điệu và tần số thở khi căng thẳng về cảm xúc đã được ghi nhận ở tất cả bệnh nhân, ngay cả khi chụp X-quang phổi. Chúng mang tính dai dẳng. Hai tuần sau khi bắt đầu điều trị bằng Grandaxin®, mức độ nghiêm trọng của họ giảm nhẹ, từ 1,8 ± 0,11 xuống 1,6 ± 0,11 điểm (p> 0,05). Chỉ số này đã giảm 1/3 vào cuối tuần thứ 4 trị liệu và là 1,2 ± 0,12 (p> 0,05). Mức độ nghiêm trọng của các triệu chứng hô hấp chủ quan vào cuối đợt điều trị bằng Grandaxin® giảm 2 lần từ 1,8 ± 0,11 xuống 0,9 ± 0,09 điểm (p <0,001), điều này nhấn mạnh sự cần thiết phải sử dụng liệu pháp giải lo âu trong điều trị phức hợp rối loạn về hô hấp thời hậu covid. Có ý nghĩa quan trọng đối với bệnh nhân là không còn cảm giác khó chịu khi hít vào và không còn cảm giác thiếu không khí, phục hồi phản ứng bình thường của hệ hô hấp trước những ảnh hưởng căng thẳng. Trong nghiên cứu của chúng tôi có 3 bệnh nhân từ bỏ ý định mua một máy đo oxy tại nhà.
Rối loạn trên đường tiêu hóa ở bệnh nhân rối loạn lo âu sau khi nhiễm coronavirus được biểu hiện bằng các triệu chứng như chán ăn, khó nuốt, cảm giác đầy bụng và đau bụng, khó chịu ở bụng, buồn nôn và nôn khi tâm lý căng thẳng, đi lỏng phân hoặc ngược lại, táo bón, mặc dù tất cả bệnh nhân đã sử dụng prebiotics và probiotics trước khi chỉ định Grandaxin® để tránh rối loạn sinh học. Cần lưu ý sự dai dẳng của rối loạn tiêu hóa. Rối loạn tiêu hóa vào cuối tuần điều trị thứ 2 chỉ giảm 12% – từ 1,97 ± 0,1 đến 1,73 ± 0,1 điểm (p> 0,05), sau 4 tuần là 1,36 ± 0,15 (p> 0,05), nhưng đến cuối tuần thứ 6 điều trị bằng Grandaxin®, mức độ nặng giảm gần 2 lần – từ 1,97 ± 0,1 xuống 1,06 ± 0,07 điểm (p <0,001). Bệnh nhân ghi nhận sự gia tăng cảm giác thèm ăn, phân bình thường. Giảm cảm giác khó chịu khi nuốt và khi thức ăn qua thực quản, giảm số lần đầy hơi, buồn nôn và nôn mửa trong thời gian căng thẳng đã biến mất. Có lẽ tác dụng của Grandaxin® đối với rối loạn dạng cơ thể trên đường tiêu hóa có liên quan đến tác động tích cực đối với cấu trúc hệ GABA-ergic và bình thường hóa trong việc phân bố thần kinh phó giao cảm bị rối loạn của đường tiêu hóa.
Rối loạn tiết niệu sinh dục liên quan đến lo âu ở bệnh nhân sau khi nhiễm coronavirus được biểu hiện bằng các triệu chứng khác nhau không liên quan đến các bệnh viêm bàng quang, thận và bộ phận sinh dục. Đến cuối quá trình điều trị, các bệnh nhân đã bình thường hóa chức năng tiết niệu, giảm mức độ nghiêm trọng của hội chứng tiền kinh nguyệt (premenstrual syndrome). Mức độ nghiêm trọng của các triệu chứng tiết niệu sinh dục đã giảm đáng kể vào cuối tuần thứ 4 trị liệu, chỉ số “rối loạn niệu sinh dục” giảm 33%, từ 2,13 ± 0,11 xuống 1,43 ± 0,12 điểm (p <0,001), và vào cuối tuần thứ 6 chỉ tiêu này giảm 2 lần – từ 2,13 ± 0,11 xuống 1,06 ± 0,11 điểm (p <0,001).
Trước khi bắt đầu điều trị bằng Grandaxin®, các rối loạn thần kinh thực vật chủ yếu biểu hiện bằng rối loạn điều hòa nhiệt, khả năng chịu nóng và lạnh kém, hiện tượng “bốc hỏa”, ớn lạnh. Sau quá trình điều trị bằng Grandaxin®, điều quan trọng nhất đối với bệnh nhân là sự biến mất của các biểu hiện chủ quan như “ớn lạnh”, cũng như sốt. Bệnh nhân ngừng đo nhiệt độ nhiều lần trong ngày. Mức độ nghiêm trọng của các rối loạn tự chủ giảm dần, đầu tiên là 2 ± 0,5 (p> 0,05) sau 2 tuần, và sau 4 tuần giảm xuống 1,56 ± 0,5 (p <0,001). Mức giảm tối đa của các rối loạn tự chủ được ghi nhận vào cuối tuần thứ 6: chẳng hạn, chỉ số thang phụ giảm hơn 2 lần từ 2,4 ± 0,11 xuống 1,1 ± 0,07 điểm (p <0,001).
Hình 2. Sự thay đổi các biểu hiện lo âu về tâm lý trong quá trình điều trị bằng thuốc Grandaxin®
Sau một liệu trình điều trị với Grandaxin®, hành vi của bệnh nhân trong quá trình kiểm tra dần bình thường trở lại: không còn lo âu, bồn chồn, khó chịu; điểm trung bình cho mục phụ “hành vi trong khi khám” giảm từ 2,47 ± 0,09 xuống 1,68 ± 0,5 (p <0,001 ) sau 4 tuần và đạt mức tối thiểu sau 6 tuần, ở mức 1,03 ± 0,09 điểm (p <0,001) (Hình 2).
KẾT LUẬN
Theo kết quả của việc đánh giá chất lượng cuộc sống của những bệnh nhân đã trải qua một đợt nhiễm coronavirus mới, mặc dù không có dấu hiệu mất khả năng lao động, ở những người được hỏi xảy ra các rối loạn tâm lý-cảm xúc (thường dưới dạng tăng lo âu cá nhân), rối loạn giấc ngủ, rối loạn hoạt động hệ tự trị, hội chứng suy nhược.
Những triệu chứng này có ý nghĩa đối với người bệnh và ảnh hưởng đáng kể đến chất lượng cuộc sống của họ, do đó, cần có một phương pháp tiếp cận tổng hợp không chỉ trong chẩn đoán lâm sàng về hậu quả lâu dài của nhiễm coronavirus chủng mới, mà còn trong việc điều chỉnh liệu pháp điều trị bằng thuốc cho họ.
Điều trị giải lo âu trên hệ GABA-ergic không chỉ hữu ích để làm giảm các biểu hiện về tâm lý, mà còn cả các biểu hiện lo âu về thần kinh thực vật, và tác dụng của Grandaxin® như một loại thuốc giảm đau có thể có tác dụng tốt trong việc giảm triệu chứng đau của bệnh.
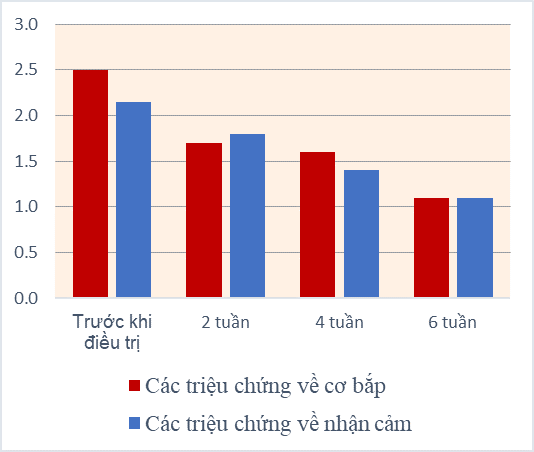
Hình 3. Sự thay đổi các triệu chứng lo âu về đau trong quá trình điều trị bằng thuốc Grandaxin®
Sau là biểu hiện hàng đầu của nhiễm coronavirus [12, 40]. Rối loạn triệu chứng cơ thể về cơ bắp được biểu hiện bằng hội chứng đau, rối loạn trương lực cơ, biểu hiện xơ cơ, co giật cơ. Những biểu hiện này đã rõ ràng trước khi bắt đầu điều trị ở một nửa số bệnh nhân. 15 người còn lại có biểu hiện ở mức trung bình. Không ghi nhận trường hợp nào không có rối loạn hoặc suy giảm mức độ nhẹ. Đến cuối tuần thứ 2 điều trị bằng Grandaxin®, mức độ nghiêm trọng của rối loạn loạn triệu chứng cơ thể về cơ bắp giảm 30% từ 2,53 ± 0,09 xuống 1,77 ± 0,09 và vào cuối tuần thứ 6 các triệu chứng cơ giảm 2,5 lần, từ 2,53 ± 0,09 xuống 1,13 ± 0,06 điểm (p <0,001) (Hình 3).
Hình 3. Sự thay đổi các triệu chứng lo âu về đau trong quá trình điều trị bằng thuốc Grandaxin®
Trái ngược với rối loạn triệu chứng cơ thể về cơ bắp, suy giảm cảm giác ban đầu đáp ứng kém hơn với các biện pháp điều trị. Mặc dù mức độ nghiêm trọng ban đầu thấp hơn, vào cuối tuần điều trị thứ 2, các biểu hiện của họ chỉ giảm 17%, từ 2,23 ± 0,1 xuống 1,86 ± 0,1 điểm (p> 0,05). Đến cuối tuần thứ 6 mức độ giảm hơn 2 lần, từ 2,23 ± 0,09 xuống 0,97 ± 0,11 điểm (p <0,001). Ngược lại với các rối loạn về cơ bắp, các rối loạn cảm giác được chấm dứt hoàn toàn ở 6 bệnh nhân (20%).
Do đó, việc điều trị các triệu chứng lo âu với Grandaxin® đã dẫn đến cải thiện đáng kể chất lượng cuộc sống của những bệnh nhân vừa trải qua một đợt nhiễm coronavirus mới.
TÀI LIỆU THAM KHẢO
- Greenhalgh T., Knight M., A’Court C., Buxton M., Husain L. Management of post-acute Covid-19 in primary care. BMJ. 2020;370:m3026. https://doi.
org/10.1136/bmj.m3026.
2. Chan A.T., Drew D.A., Nguyen L.H., Joshi A.D., Ma W., Guo C.G. et. al. COPE Consortium. The Coronavirus Pandemic Epidemiology (COPE) Consortium: A Call to Action. Cancer Epidemiol Biomarkers Prev. 2020;29(7):1283–1289. https://doi.org/10.1158/1055-9965.EPI-20-0606.
3. Dani M., Dirksen A., Taraborrelli P., Torocastro M., Panagopoulos D., Sutton R., Lim P.B. Autonomic dysfunction in “long COVID”: rationale, physiology and management strategies. Clin Med (Lond). 2021;21(1):e63–e67. https://doi. org/10.7861/clinmed.2020-0896.
4. Kroenke K., Spitzer R.L., Williams J.B., Monahan P.O., Löwe B. Anxiety disorders in primary care: prevalence, impairment, comorbidity, and detection.
Ann Intern Med. 2007;146(5):317–325. https://doi.org/10.7326/0003-4819- 146-5-200703060-00004.
5. Goldstein D.S. The extended autonomic system, dyshomeostasis, and COVID-19. Clin Auton Res. 2020;30(4):299–315. https://doi.org/10.1007/
s10286-020-00714-0.
6. Fudim M., Qadri Y.J., Ghadimi K., MacLeod D.B., Molinger J., Piccini J.P. et al. Implications for Neuromodulation Therapy to Control Inflammation and Related Organ Dysfunction in COVID-19. J Cardiovasc Transl Res. 2020;13(6):894–899. https://doi.org/10.1007/s12265-020-10031-6.
7. Staedtke V., Bai R.Y., Kim K., Darvas M., Davila M.L., Riggins G.J. et al. Disruption of a self-amplifying catecholamine loop reduces cytokine
release syndrome. Nature. 2018;564(7735):273–277. https://doi.org/ 10.1038/s41586-018-0774-y.
8. Guilmot A., Maldonado Slootjes S., Sellimi A., Bronchain M., Hanseeuw B., Belkhir L. et al. Immune-mediated neurological syndromes in SARS-CoV-2-
infected patients. J Neurol. 2021;268(3):751–757. https://doi.org/10.1007/ s00415-020-10108-x.
9. Ruzieh M., Batizy L., Dasa O., Oostra C., Grubb B. The role of autoantibodies in the syndromes of orthostatic intolerance: a systematic review. Scand
Cardiovasc J. 2017;51(5):243–247. https://doi.org/10.1080/14017431.2017.1 355068.
10. Li H., Kem D.C., Reim S., Khan M., Vanderlinde-Wood M., Zillner C. et al. Agonistic autoantibodies as vasodilators in orthostatic hypotension:
a new mechanism. Hypertension. 2012;59(2):402–408. https://doi.org/ 10.1161/HYPERTENSIONAHA.111.184937.
11. Chigr F., Merzouki M., Najimi M. Autonomic Brain Centers and Pathophysiology of COVID-19. ACS Chem Neurosci. 2020;11(11):1520– 1522. https://doi.org/10.1021/acschemneuro.0c00265.
12. Carfi A., Bernabei R., Landi F. Рersistent symptoms in patients after acute COVID-19. JAMA. 2020;324(6):603–605. https://doi.org/10.1001/
jama.2020.12603.
13. El Sayed S., Shokry D., Gomaa S.M. Post-COVID-19 fatigue and anhedonia: A cross-sectional study and their correlation to post-recovery period. Neuropsychopharmacol Rep. 2021;41(1):50–55. https://doi.org/10.1002/ npr2.12154.
14. Ferraro F., Calafiore D., Dambruoso F., Guidarini S., de Sire A. COVID-19 related fatigue: Which role for rehabilitation in post-COVID-19 patients?
A case series. J Med Virol. 2021;93(4):1896–1899. https://doi.org/10.1002/ jmv.26717.
15. Ortelli P., Ferrazzoli D., Sebastianelli L., Engl M., Romanello R., Nardone R. et al. Neuropsychological and neurophysiological correlates of fatigue
in post-acute patients with neurological manifestations of COVID-19: insights into a challenging symptom. J Neurol Sci. 2021;420:117271. https://doi.org/10.1016/j.jns.2020.117271.
16. Townsend L., Dyer A.H., Jones K., Dunne J., Mooney A., Gaffney F. et al. Persistent fatigue following SARS-CoV-2 infection is common and independent of severity of initial infection. PLoS One. 2020;15(11):е0240784. https://doi.org/10.1371/journal.pone.0240784.
17. Helms J., Kremer S., Merdji H., Clere-Jehl R., Schenck M., Kummerlen C. et al. Neurologic Features in Severe SARS-CoV-2 Infection. N Engl
J Med. 2020;382(23):2268–2270. https://doi.org/10.1056/nejmc2008597. - Benussi A., Di Lorenzo F., Dell’Era V., Cosseddu M., Alberici A., Caratozzolo S. et al. Transcranial magnetic stimulation distinguishes Alzheimer disease from frontotemporal dementia. Neurology. 2017;89(7):665–672. https://doi.org/10.1212/WNL.0000000000004232.
19. Sumner P., Edden R.A., Bompas A., Evans C.J., Singh K.D. More GABA, less distraction: a neurochemical predictor of motor decision speed. Nat
Neurosci. 2010;13(7):825–827. https://doi.org/10.1038/nn.2559.
20. Porges E.C., Woods A.J., Edden R.A., Puts N.A., Harris A.D., Chen H. et al. Frontal gamma-aminobutyric acid concentrations are associated with
cognitive performance in older adults. Biol Psychiatry Cogn Neurosci Neuroimaging. 2017;2(1):38–44. https://doi.org/10.1016/j.bpsc.2016.06.004 - Versace V., Sebastianelli L., Ferrazzoli D., Romanello R., Ortelli P., Saltuari L. et al. Intracortical GABAergic dysfunction in patients with fatigue and
dysexecutive syndrome after COVID-19. Clin Neurophysiol. 2021;132(5):1138–1143. https://doi.org/10.1016/j.clinph.2021.03.001.
22. Stellwagen D., Malenka R.C. Synaptic scaling mediated by glial TNF-α Nature. 2006;440(7087):1054–1059. https://doi.org/10.1038/
nature04671.
23. Nikbakht F., Mohammadkhanizadeh A., Mohammadi E. How does the COVID-19 cause seizure and epilepsy in patients? The potential
mechanisms. Mult Scler Relat Disord. 2020;46:102535. Avialable at: https://pubmed.ncbi.nlm.nih.gov/33010584/.
24. Tian J., Milddleton B., Kaufman D.L. GABA administration prevents severe illness and death following coronavirus infection in mice. bioRxiv.
2020:2020.10.04.325423. https://doi.org/10.1101/2020.10.04.325423.
25. Baller E.B., Hogan C.S., Fusunyan M.A., Ivkovic A., Luccarelli J.W., Madva E. et al. Neurocovid: Pharmacological Recommendations for Delirium
Associated with COVID-19. Psychosomatics. 2020;61(6):585–596. https://doi.org/10.1016/j.psym.2020.05.013.
26. Смулевич А.Б., Дробижев М.Ю., Иванов С.В. Клинические эффекты бензодиазепиновых транквилизаторов в психиатрии и общей медицине.
М.: Медиа-Сфера; 2005. 88 с. Режим доступа: https://otherreferats.allbest.ru/medicine/00516644_0.html.
27. Bandelow B., Sher L., Bunevicius R., Hollander E., Kasper S., Zohar J. et al. Guidelines for the pharmacological treatment of anxiety disorders,
obsessive-compulsive disorder and posttraumatic stress disorder in primary care. Int J Psychiatry Clin Pract. 2012;16(2):77–84. https://doi.org/10.3
109/13651501.2012.667114.
28. Корнеева А. Безопасное лечение стрессогенных расстройств в практике психиатров и психологов. Лечащий врач. 2018;(6):22. Режим доступа:
https://www.lvrach.ru/partners/grandaxin/15437004.
29. Дума С.Н., Лисиченко О.В., Лукьянова Г.В. Психовегетативные, астенические и когнитивные нарушения при дисплазии
соединительной ткани: выбор оптимальной терапии. Фарматека.
2012;(7):131–135. Режим доступа: https://pharmateca.ru/ru/archive/article/8436. 30. Густов А.В., Александрова Е.А., Паршина Е.В., Бородачева И.В.,
Беляков К.М. Эффективность Сертралина в качестве ко-анальгетика при хронических болевых синдромах нижней части спины. Международный
журнал прикладных и фундаментальных исследований. 2016;8(2):158–
161. Режим доступа: https://www.applied-research.ru/ru/article/ view?id=9995.
31. Sierralta F., Miranda H.F. Analgesic effect of benzodiazepines and flumazenil. Gen Pharmacol. 1992;23(4):739–742. https://doi.org/10.1016/0306-
3623(92)90158-g.
32. Dolezal T., Krsiak M. Augmentation of analgesic effect of ibuprofen by alprazolam in experimental model of pain. Physiol Res. 2002;51(2):179–
184. Available at: https://pubmed.ncbi.nlm.nih.gov/12108928/.
33. Rad R.E., Ghaffari F., Fotokian Z., Ramezani A. The effectiveness of ibuprofen and lorazepam combination therapy in treating the symptoms
of acute Migraine: A randomized clinical trial. Electron Physician.
2017;9(3):3912–3917. https://doi.org/10.19082/3912.
34. Talarek S., Fidecka S. Role of nitric oxide in benzodiazepines-induced
antinociception in mice. Pol J Pharmacol. 2002;54(1):27–34. Available at: https://pubmed.ncbi.nlm.nih.gov/12020041/.
35. Jiménez-Velázquez G., López-Muñoz F.J., Fernández-Guasti A. Participation of the GABA/benzodiazepine receptor and the NO-cyclic GMP pathway
in the “antinociceptive-like effects” of diazepam. Pharmacol Biochem Behav. 2008;91(1):128–133. https://doi.org/10.1016/j.pbb.2008.06.021.
36. Green S.J. Covid-19 accelerates endothelial dysfunction and nitric oxide deficiency. Microbes Infect. 2020;22(4–5):149–150. https://doi.org/10.1016/
j.micinf.2020.05.006.
37. Martel J., Ko Y.F., Young J.D., Ojcius D.M. Could nasal nitric oxide help to mitigate the severity of COVID-19? Microbes Infect. 2020;22(4–5):168–171.
https://doi.org/10.1016/j.micinf.2020.05.002.
38. Wu R., Wang L., Kuo H.D., Shannar A., Peter R., Chou P.J. et al. An Update on Current Therapeutic Drugs Treating COVID-19. Curr Pharmacol Rep.
2020;1–15. https://doi.org/10.1007/s40495-020-00216-7.
39. Adusumilli N.C., Zhang D., Friedman J.M., Friedman A.J. Harnessing nitric oxide for preventing, limiting and treating the severe pulmonary consequences of COVID-19. Nitric Oxide. 2020;103:4–8. https://doi.org/10.1016/j. niox.2020.07.003.
40. Shanthanna H., Strand N.H., Provenzano D.A., Lobo C.A., Eldabe S., Bhatia A. et al. Caring for patients with pain during the COVID-19 pandemic: consensus recommendations from an international expert panel. Anaesthesia. 2020;75(7):935–944. https://doi.org/10.1111/anae.15076